|
BTK抑制剂(BTKi)的出现为广大淋巴瘤患者带来了新的治疗生机与希望,现已成为CLL/SLL、R/R MCL和WM的标准治疗方案。然而,对于需要长期接受BTKi治疗的惰性淋巴瘤患者,因不良事件(AE)而导致的BTKi停药越来越成为影响患者生存获益的重要因素。 在第62届美国血液学年会(2020ASH)和第26届欧洲血液学协会年会(2021EHA)上连续报道了针对既往BTKi(伊布替尼和/或阿卡替尼)不耐受的复发/难治B细胞恶性肿瘤患者(CLL/SLL、MCL、MZL或WM)接受泽布替尼治疗的单臂、开放、多中心II期研究(NCT04116437;BGB-3111-215)1,2。研究显示,在既往BTKi不耐受的患者中泽布替尼表现出良好的耐受性和疗效,既往BTKi相关的AE大部分没有发生。基于此研究,泽布替尼获得NCCN指南(2021v3)3推荐用于对其他BTKi不耐受的初治及复发/难治CLL/SLL患者。
在今年ASH会议中,研究者对这一研究数据4进行了更新。小编找到一篇中国医学科学院血液病医院邱录贵教授对此研究的点评,分享给需要的病友。
研究背景 泽布替尼是新一代BTKi,通过创新优化分子结构,有效地提高了药物的安全性。应用激酶谱分析揭示了BTKi安全性差异的潜在机制。泽布替尼对激酶具有高度选择性,优于伊布替尼、阿卡替尼、M27(阿卡替尼的主要代谢产物),而与奥布替尼相当。在对370种激酶进行的分析中,5种BTKi抑制率>50%的激酶数量分别为泽布替尼7、伊布替尼17、阿卡替尼15、M27 23、奥布替尼5。而5种BTKi的IC50分别是:泽布替尼 0.71±0.09nM、伊布替尼 0.32±0.09nM、阿卡替尼 24±9.2nM、M27 63±28nM、奥布替尼 15±5.5nM。
更低的IC50、更少的激酶靶点意味着脱靶效应更少见。基于这样的结构优势,泽布替尼或许能为伊布替尼或阿卡替尼不耐受的患者带来新的治疗希望。

研究方法 既往接受伊布替尼和/或阿卡替尼不耐受而非出现疾病进展的患者接受泽布替尼160mg bid或320mg qd直至疾病进展或不可耐受毒性。依据患者既往接受BTKi类型分成2个队列:队列1为接受伊布替尼不耐受患者,队列2为接受仅阿卡替尼或阿卡替尼和伊布替尼不耐受患者。
不耐受事件定义为发生研究者认为不可接受的毒性,尽管采取了最佳支持治疗,但仍由于以下原因之一而停止治疗:≥2级非血液学毒性持续>7天,≥3级非血液学毒性持续任何时间,3级中性粒细胞减少症伴感染或发热,4级血液学毒性持续研究者认为应停止BTKi治疗。开始泽布替尼治疗前需待毒性缓解至≤1级或基线水平。

△ 研究设计
研究结果 截至2021年9月8日(截止日期),57例患者被纳入队列1(44例CLL/SLL、9例 WM、2例MCL、2例MZL);10例患者被纳入队列2(6例CLL/SLL、2例WM、1例MCL、1例MZL)。队列1中位年龄为71.0岁(范围49-91岁),队列2中位年龄为73.5岁(范围65-83岁)。队列1的中位治疗持续时间为11.6月(范围0.6-20.3月),队列2的中位治疗持续时间为9.8月(范围0.5-12.0月)。
至截止日期,56例(83.6%)患者仍在治疗中。11例患者停止治疗,5例因不良事件而停药,4例因疾病进展,1例研究者决定,1例撤回知情同意。

△ 患者基线特征

△ 患者停药情况
70.4%(81/115)伊布替尼不耐受事件在接受泽布替尼后未再发生,再次发生的34起中26起(76.5%)为更低级别;65.8%(25/38)伊布替尼的3级不耐受事件在接受泽布替尼后未再发生。83.3%(15/18)阿卡替尼不耐受事件在接受泽布替尼后未再发生,再次发生的3起中1起(33%)为更低级别;75.0%(3/4)阿卡替尼的3级不耐受事件在接受泽布替尼后未再发生。所有4级不耐受事件在接受泽布替尼治疗后未再发生。
59.6%(34/57)的伊布替尼治疗组患者和70.0%(7/10)的阿卡替尼治疗组患者没有再发生任何不耐受事件。无1例患者发生更高级别的既往BTKi不耐受事件。

△ 不良事件复发情况
在所有疗效可评估的患者中,疾病控制率(DCR)为93.8%(60/64),ORR率(PR或更好)为64.1%(41/64)。
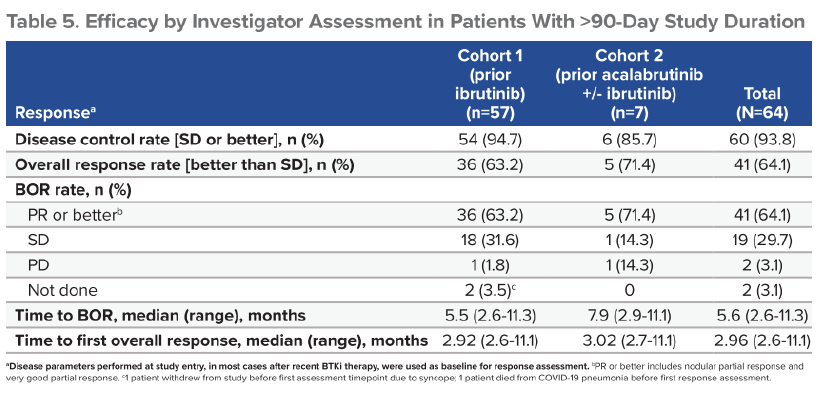
△ 疗效数据
研究结论 泽布替尼在既往BTKi不耐受的患者中表现出良好的疗效和耐受性,既往BTKi相关的AE大部分没有发生或严重程度降低,同时没有发生任何加重的复发事件。患者在换用泽布替尼以后,治疗效果也得到了很好地保证,93.8%的患者疾病得到了控制,64.1%的患者疗效改善。这些数据表明对既往BTKi治疗不耐受淋巴瘤患者,泽布替尼是一种可靠的治疗选择。
专家点评 泽布替尼是新一代BTKi,通过创新优化分子结构,成为目前唯一在外周血和淋巴结都实现了100%抑制的BTKi。泽布替尼低IC50、较少激酶靶点的特性使得其靶点选择性更强且脱靶效应更低,可以最大程度降低脱靶作用,带来更好的安全性。
此前在泽布替尼头对头对比伊布替尼治疗MYD88突变型的WM 患者3期研究(ASPEN)5中,已发现泽布替尼在安全性和耐受性方面更具优势:泽布替尼导致死亡、停药或治疗中断的AE更少。而在泽布替尼头对头对比伊布替尼治疗CLL/SLL患者的3期研究(ALPINE)6中,同样发现停止治疗相关AE及致死性AE伊布替尼的发生率均高于泽布替尼。这些全球多中心随机对照临床研究证明了药物结构的优化可转化为临床疗效和安全性的优势。
BGB-3111-215临床研究进一步回答了已接受伊布替尼和/或阿卡替尼后出现不良事件的患者应该如何进行临床治疗选择。随着患者更长随访数据的披露,我们发现患者的绝大部分不良事件未发生复发,仅有的少部分复发事件也多呈现减轻趋势,没有发生任何加重的复发事件。这一结果已经充分证明了泽布替尼的安全性。而疗效数据也显示了换用泽布替尼为患者带来的获益,64.1%的ORR率(PR或更好)证明了即使出现BTKi不耐受之后换药仍然可以取得更好的的临床疗效。
作为我国首个“出海”的淋巴瘤靶向治疗本土新药,泽布替尼当前已经在美国、中国、欧盟、阿联酋、加拿大、澳大利亚等40个国家和地区获得上市批准,并得到美国NCCN指南与中国CSCO临床指南推荐。泽布替尼用于一线CLL/SLL治疗的3期研究数据(SEQUOIA)也在本届ASH上发表,和传统的BR相比,有显著优势,为其更广泛地用于淋巴瘤患者提供了新的循证依据。目前泽布替尼已经被纳入我国医保,药品价格明显降低,药物可及性进一步提高,让更多淋巴瘤患者能够从具有国际品质的国产抗癌新药中获益。
专家介绍

邱录贵 教授 中国医学科学院血液病医院淋巴瘤诊疗中心主任
参考文献: 1. 2020 ASH poster 2947 2. 2021 EHA abstract #EP642 3. 2021v3 NCCN-CLL指南 4. 2021 ASH poster 1410 5. 2020 ASCO. Oral Abstract#8007. 6. 2021 EHA Oral Abstract# LB1900
|  /1
/1 