- 主题
- 598
- 您的身份
- 家属
- 就诊医院
- 307
- 病理报告
- 弥漫大B细胞
- 目前状态
- 天堂
参加活动:0 次 组织活动:8 次
您的身份家属
病理报告弥漫大B细胞
就诊医院307
目前状态天堂
最后登录2025-4-2

|
资讯摘要
1、2019年6月,复发难治弥漫大B淋巴瘤领域一款ADC药物Polatuzumab(Pola)获FDA批准上市,成为全球获批的第五个ADC药物。
2、PRIMA研究10年随访结果显示滤泡淋巴瘤免疫化疗后进行利妥昔单抗(美罗华)维持治疗可以使近一半患者10年内持续无疾病进展或无死亡。
1)Pola新药
什么是ADC药物
ADC是抗体-药物偶联物的简称,由抗体、细胞毒药物通过连接体连接而成。
ADC将抗体的靶向性与细胞毒药物的抗肿瘤作用结合,降低细胞毒药物的不良反应,提高肿瘤治疗选择性,更好地应对靶向单抗的耐药问题。
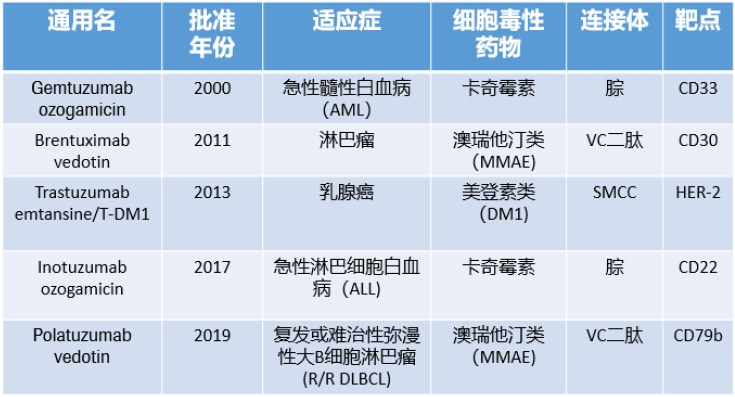
全球获批ADC药物
2019年6月,ADC药物Polatuzumab在复发难治弥漫领域获FDA批准上市,成为全球获批的第五个ADC药物。
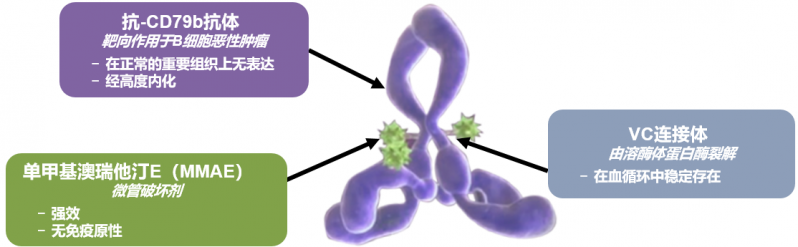
ADC药物Pola
Polatuzumabvedotin(简称Pola)是一种ADC,由人源化抗CD79b抗体与微管蛋白聚合抑制剂(MMAE)通过连接体偶联而成。在与B细胞表面的CD79b结合之后,Pola发生内化,连接体发生裂解并将MMAE释放到细胞内,由后者发挥抑制细胞分裂并诱导凋亡的作用。
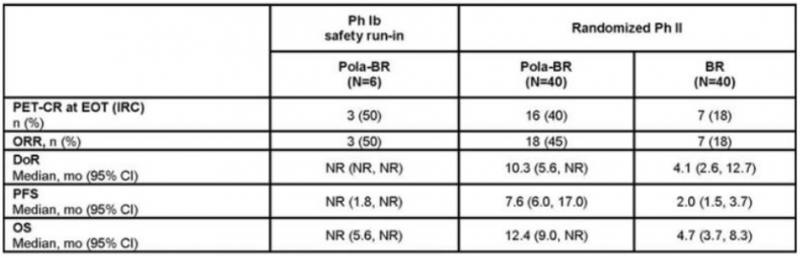
2019年6月,FDA批准Pola与苯达莫司汀+利妥昔单抗(Pola-BR)联合治疗已至少接受两种既往治疗的R/R DLBCL成人患者。该获批基于一项1b/2期临床试验数据,Pola-BR组完全缓解率是BR组的2倍以上(40%vs.18%;p=0.026), Pola-BR组显著延长DoR(HR,0.44;p=0.032)、PFS(HR,0.34;p<0.0001)和OS(HR,0.42;p=0.0023)。
2)维持用药
PRIMA临床研究
PRIMA研究(NCT00140582)是第一个评估FL患者一线免疫化疗后利妥昔单抗(R)维持治疗的III期研究。3年/6年随访结果均显示R维持治疗显著改善PFS,各亚组结果一致。
研究设计
既往未经治疗的高肿瘤负荷FL患者非随机接受(R-CHOP/R-CVP/R-FCM)诱导治疗。1018名患者完成诱导治疗,随机分为R维持(n=505)或观察组(n=513)。
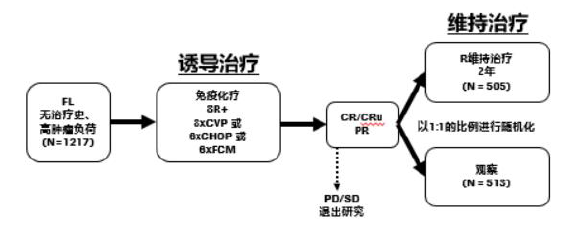
研究结果
1、R维持治疗显著延长PFS。
两组中位PFS分别为10.5年vs. 4.1年(HR=0.61;95%CI 0.52-0.73;p<0.001)。
两组10年PFS估计分别为51.1%vs.35%。
根据年龄、性别、FLIPI评分、诱导方案、诱导反应情况分层,维持治疗显示一致的PFS获益。
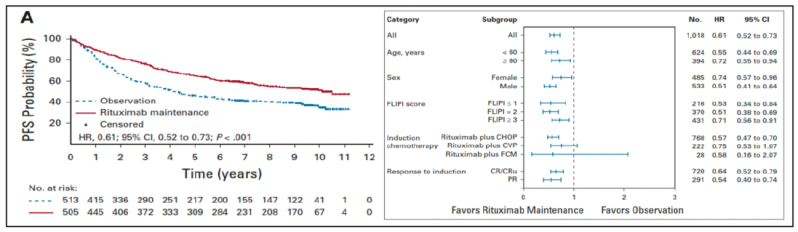
2、R维持治疗显著改善至下次治疗时间(TTNLT)及至下次化疗时间(TTNCT)
R维持组中位TTNLT未达到,观察组为6.1年(HR=0.66,95CI0.55-0.78,P<0.001)。
10年TTNLT估计分别为53.4%vs.41.2%。
R维持组中位TTNCT未达到,观察组为9.3年(HR=0.71,95%CI 0.59-0.86,P<0.001)。
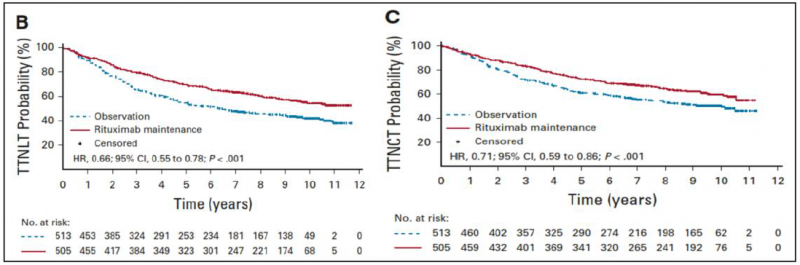
3、10年OS两组未见显著差异。
两组OS分别为80.1%vs.79.9%,两组中位OS均未观察到。
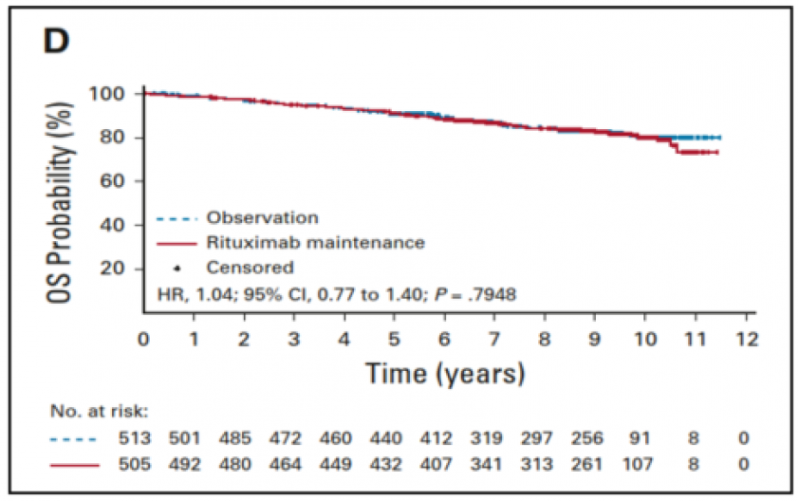
4、安全性结果
R维持治疗组患者3-4级不良事件(AE)发生率更高,严重不良事件(SAE)分别为21.2%vs.13.4%,主要由血细胞减少(5.2% v 1.6%)和感染(4.4% v 1.0%)造成。最常见的3-4级AE是良性/恶性/性质不明肿瘤(包括囊肿和息肉)(两组均4%左右)。两组致死性AE分别为1.6%和0.6%。
随机分组后R维持组88名(17.4%)患者死亡,观察组84名(16.4%)患者死亡。最常见的死亡原因是疾病进展(两组分别为51.1%vs. 47.6%)和继发实体肿瘤(两组分别为5.7%vs. 20.2%)。
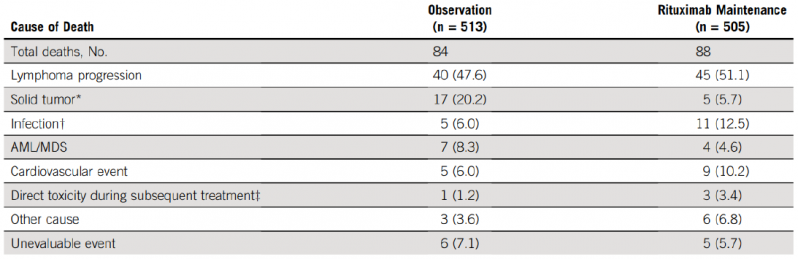
引发思考
1、从临床角度,PRIMA研究结果意味着免疫化疗后R维持治疗可以使近一半的患者10年内持续无疾病进展或无死亡,未需进一步抗淋巴瘤治疗。
2、观察组因继发肿瘤引起的死亡几乎是R维持组的4倍。可能原因是反复使用细胞毒药物和放疗增加了继发肿瘤的发生率。相反,R维持组因感染引起的死亡是观察组的2倍。长期随访未观察到新的安全性信号。
3、PFS是否能作为OS的替代终点仍存在争议。统计模型显示,PFS和OS的相关性在进展后长期生存的恶性肿瘤(比如FL)中相关性更弱,这解释了PFS优势可能在后续治疗后被稀释。
|
|
 /1
/1 